Nguồn gốc
Khi các electron trong nguyên tử bị kích thích, ví dụ như bằng cách nung nóng, năng lượng bổ sung sẽ đẩy các electron lên các orbital năng lượng cao hơn. Khi các electron rơi xuống và để lại trạng thái kích thích, năng lượng sẽ được phát lại dưới dạng photon. Bước sóng (hoặc tương đương, tần số) của photon được xác định bởi sự khác biệt về năng lượng giữa hai trạng thái. Những photon phát ra này tạo nên quang phổ của phần tử.
Thực tế chỉ có một số màu nhất định xuất hiện trong phổ phát xạ nguyên tử của nguyên tố có nghĩa là chỉ phát ra một tần số nhất định của ánh sáng. Mỗi tần số này liên quan đến năng lượng theo công thức:
Trong đó E là photon, là năng lượng của photon, là tần số của nó, và là hằng số Planck . Điều này kết luận rằng chỉ có các photon với năng lượng cụ thể được phát ra bởi nguyên tử. Nguyên lý của phổ phát xạ nguyên tử giải thích các màu khác nhau trong các dấu hiệu của neon, cũng như kết quả kiểm tra ngọn lửa hóa học (được mô tả dưới đây).
Các tần số của ánh sáng mà một nguyên tử có thể phát ra phụ thuộc vào các trạng thái mà các điện tử có thể được đưa vào. Khi bị kích thích, một điện tử chuyển sang mức năng lượng cao hơn hoặc quỹ đạo. Khi electron rơi xuống mức nền của nó thì ánh sáng phát ra.

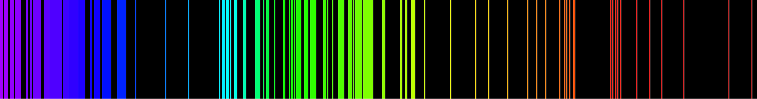
Hình trên cho thấy phổ phát xạ ánh sáng khả kiến đối với hydro. Nếu chỉ có một nguyên tử hydro, thì chỉ có một bước sóng duy nhất sẽ được quan sát tại một thời điểm nhất định. Một số lượng phát thải có thể được quan sát bởi vì mẫu chứa nhiều nguyên tử hydrogen ở các trạng thái năng lượng ban đầu khác nhau và đạt đến trạng thái năng lượng cuối cùng khác nhau. Những sự kết hợp khác nhau dẫn đến phát thải đồng thời ở các bước sóng khác nhau.