Đo độ phức tạp (EDTA)
Các phép đo nhiệt độ sử dụng muối natri của axit ethylenediaminetetra-acetic (EDTA) đã được chứng minh để xác định một loạt các ion kim loại. Ống ngưng phản ứng khiêm tốn là khiêm tốn, vì vậy việc chuẩn độ thường được thực hiện với nồng độ dung dịch 1 mol / L. Điều này đòi hỏi việc sử dụng muối tetra-natri của EDTA chứ không phải là muối di-nat thông thường được bão hòa ở nồng độ chỉ khoảng 0,25 mol / L.
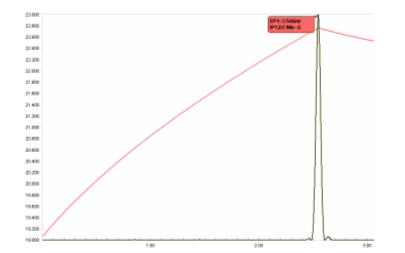
Một ứng dụng xuất sắc là sự xác định tuần tự của canxi và magiê. Mặc dù canxi phản ứng tỏa nhiệt với EDTA (nhiệt của chelation ~ -23,4 kJ / mol), magiê phản ứng với endothermically với một nhiệt của chelation ~ 20,1 kJ / mol. Điều này được minh họa trong cốt truyện của EDTA với canxi và magiê trong nước biển (Hình 18). Tiếp theo là đường cong nhiệt độ của dung dịch, điểm dừng cho hàm lượng canxi (điểm cuối đuôi được gắn màu đỏ) được theo sau bởi một vùng tăng nhiệt độ khiêm tốn do sự cạnh tranh giữa nhiệt độ pha loãng của dung dịch với dung dịch và phản ứng nhiệt của Mg2 + và EDTA . Điểm dừng cho tiêu thụ Mg2 + (điểm cuối được gắn màu xanh) bởi EDTA được tiết lộ bằng cách tăng nhiệt độ gây ra hoàn toàn do nhiệt độ pha loãng.
Hình 15. Mạch điều chỉnh việc chuẩn độ dư thừa EDTA với Cu (II) trong dung dịch đệm NH3 / NH4Cl
Tiêu chuẩn EDTA trực tiếp với các ion kim loại có thể thực hiện được khi phản ứng nhanh, ví dụ kẽm, đồng, canxi và magiê. Tuy nhiên, với động học phản ứng chậm hơn như được thể hiện bằng coban và niken, việc chuẩn độ lại được sử dụng. Phản ứng cho coban và niken được thực hiện trong môi trường amoniac; đệm với amoniac: dung dịch clorua amoni. Một dư thừa của EDTA được thêm vào, và được chuẩn độ lại với dung dịch Cu (II). Người ta giả định rằng điểm ngắt được tiết lộ bởi sự khác biệt giữa êlectri phản ứng giữa sự hình thành phức hợp Cu-EDTA, và sự hình thành của phức Cu-amin.

Hình 16. Xác định độ tinh khiết EDTA nhiệt của dấu Cu (II) bằng cách xúc tác Mn (II) phản ứng tỏa nhiệt giữa hydrogen peroxide và polyhydric phenol.
Một thủ tục đầu cuối xúc tác để xác định lượng vết của ion kim loại trong dung dịch (khoảng 10 mg / L) sử dụng 0,0 mol 0,0 mol / L EDTA. Điều này đã được áp dụng để xác định mức Cu (II) ở mức thấp trong các bồn mạ chuyên dụng, và để xác định độ cứng tổng trong nước. Phản ứng entalpies của EDTA với hầu hết các ion kim loại thường khá thấp, và thường có nồng độ chuẩn độ khoảng 1 mol / L được sử dụng với số tiền tương xứng cao của titrand để có được những điểm kết thúc có thể tái tạo. Sử dụng một điểm cuối được chỉ định xúc tác, có thể sử dụng nồng độ chuẩn EDTA rất thấp. Đáp lại độ chuẩn được sử dụng. Một dư thừa của EDTA giải pháp được thêm vào. Sự dư thừa của EDTA được gia tốc bằng một ion kim loại thích hợp như Mn2 + hoặc Cu2 +. Ở điểm cuối, sự vượt quá đầu tiên của ion kim loại xúc tác mạnh phản ứng giữa phenol polyhdric (như resorcinol) và hydrogen peroxide.
Chiết áp lượng mưa
Phép đo nhiệt độ đặc biệt phù hợp với việc xác định một loạt các chất phân tích, nơi một chất kết tủa được hình thành bằng phản ứng với chất thử. Trong một số trường hợp, có thể cung cấp một phương pháp thay thế cho phương pháp chuẩn độ chẩn đoán thông thường. Trong các trường hợp khác, các hóa chất phản ứng có thể được sử dụng mà không có tương đương thỏa đáng trong phép chuẩn potentiometric.
Các phản ứng với bạc nitrate
Sự chuẩn độ nhiệt của bạc nitrat với halogenua và xianua là tất cả. Phản ứng của bạc nitrat với clorua là tỏa nhiệt. Ví dụ, enthalpy phản ứng của Ag + với Cl- là cao -61,2 kJ / mol. Điều này cho phép xác định thuận lợi về clorua với dung lượng 0,1 mol / L AgNO3. Điểm cuối rất sắc nét, và cẩn thận, có thể phân tích nồng độ clorid xuống 15 mg / L. Bromua và Clorua có thể được xác định trong hỗn hợp.
Chuẩn độ của sulfat
Sulfate có thể được điều chỉnh nhiệt độ nhanh và dễ dàng bằng các dung dịch tiêu chuẩn của Ba2 + như dung dịch chuẩn. Về mặt công nghiệp, thủ tục đã được áp dụng cho việc xác định sulfat trong nước muối (kể cả muối điện phân), trong các dung dịch tinh chế niken và đặc biệt đối với sulfat trong axit phosphoric ướt, ở đó nó đã được chứng minh là khá phổ biến. Quy trình này cũng có thể được sử dụng để hỗ trợ phân tích các hỗn hợp acid phức tạp có chứa axit sulfuric ở những nơi sử dụng để chuẩn độ trong môi trường không dung dịch nước là không khả thi.
Enzymal phản ứng cho sự hình thành của bari sulfat là một khiêm tốn -18,8 kJ / mol. Điều này có thể đặt một giới hạn về giới hạn dưới của sulfat trong một mẫu có thể được phân tích.
Nhiệt độ của nhôm với chất florua
Nhiệt độ chuẩn độ cung cấp một phương pháp nhanh chóng, chính xác cao để xác định nhôm trong dung dịch. Một dung dịch nhôm được điều chế với dung dịch đệm axetat và sự dư thừa của ion natri và kali. Phản ứng với natri hoặc kali fluoride tạo ra lượng mưa cực nóng của muối nhôm fluorin không hòa tan.
Al3 + + Na + + 2K + + 6F- ↔ K2NaAlF6 ↓
Bởi vì 6 mol fluoride phản ứng với một mol nhôm, việc chuẩn độ là đặc biệt chính xác, và một hệ số phương sai (CV) là 0,03 đã đạt được trong phân tích phèn.
Khi ion nhôm (được gọi là nhôm nitrat) được sử dụng làm chất chuẩn, fluoride có thể được xác định bằng cách sử dụng cùng một loại hóa học. Việc chuẩn độ này rất hữu ích trong việc xác định fluoride trong các hỗn hợp acid phức tạp được sử dụng làm etchant trong ngành bán dẫn.
Phản ứng của tổng orthophosphat
Ion orthophosphate có thể thuận tiện điều chỉnh nhiệt độ với các ion magiê trong sự có mặt của ion amoni. Một mẫu thử mẫu được đệm khoảng pH10 với dung dịch NH3 / NH4Cl.
Các phản ứng:
Mg2 + + NH4 + + PO43- ↔ MgNH4PO4 ↓
Là tỏa nhiệt. CV của dưới 0,1 đã đạt được trong các ứng dụng thử nghiệm. Thủ tục này phù hợp cho việc xác định orthophosphate trong phân bón và các sản phẩm khác.
Sự chuẩn độ của niken
Nickel có thể được chuẩn độ bằng nhiệt độ bằng cách sử dụng natri dimethylglyoximate di-như dung nhuyễn. Hóa học tương tự như phương pháp xác định trọng lực cổ điển, nhưng thời gian để xác định có thể giảm từ nhiều giờ xuống còn vài phút. Các nhiễu tiềm ẩn cần được xem xét.
Aaaathermo cat anion surf.jpg
Chuẩn độ các chất hoạt động bề mặt anion và cation
Các chất hoạt động bề mặt chứa anion và cation có thể được xác định bằng nhiệt độ bằng cách tiệt trùng một loại với chất khác. Ví dụ, benzalkonium clorua (chất hoạt động bề mặt cation cation thứ bậc) có thể được xác định trong chất tẩy rửa và tảo cho bể bơi và spa bằng cách chuẩn độ bằng dung dịch natri dodecyl sulfate chuẩn. Ngoài ra, chất hoạt động bề mặt anion như lauryl sunfat natri có thể được điều chỉnh bằng cetyl pyridinium clorua.

Hình 18. Phép chuẩn độ nhiệt của chất hoạt động bề mặt không ion trong công thức có chứa chất hoạt động bề mặt anion.
Phản ứng của chất hoạt động bề mặt không ion
Khi một dư thừa của Ba2 + được thêm vào một chất hoạt động bề mặt không ion của loại alkyl propylene oxide derivative, một phức hợp cation-cation được hình thành. Điều này có thể được điều chỉnh bằng natri tetraphenylborat tiêu chuẩn. Hai mol tetraphenylborat phản ứng với một mol của phức hợp chất hoạt động bề mặt Ba2 / không ion.
Các chế độ dung dịch nước khác
Hình 19. Phép định lượng xác định florua với axit boric
Chuẩn độ chất florua với axit boric
Các dung dịch axit fluoride (bao gồm axit flofluoric) có thể được xác định bằng cách chuẩn độ nhiệt bằng đơn giản với axit boric.
B (OH) 3 + 3F- + 3H + ↔ BF3 + 3H2O
Chu trình chuẩn độ được minh họa trong Hình 19 cho thấy điểm đầu cuối khá tròn, cho thấy rằng phản ứng có thể không tiến tới trạng thái cân bằng độ cân bằng. Tuy nhiên, vì các vùng của đường cong nhiệt độ ngay trước và sau điểm cuối là khá tuyến tính, đạo hàm thứ hai của đường cong này (đại diện cho giao điểm tiếp tuyến) sẽ xác định chính xác điểm cuối. Thật vậy, độ chính xác tuyệt vời có thể thu được với phép chuẩn độ này, với một CV ít hơn 0,1.
Xác định formaldehyde
Formaldehyde có thể được xác định bằng các dung dịch mạ không đồng vị bằng cách thêm vào một dung dịch natri sulfite dư thừa và khử ion hydroxyl được giải phóng bằng axit tiêu chuẩn.
H2C = O + HSO3- + H2O → [HO-CH2-SO3-] + O