Phenolphthalein là một hợp chất hóa học có công thức C20H14O4 và thường được viết bằng chữ “HIn” hoặc “phph” trong ký hiệu viết tắt. Phenolphthalein thường được sử dụng như là một chỉ thị trong việc chuẩn độ axit-bazơ. Đối với ứng dụng này, nó chuyển không màu trong dung dịch acid và các dung dịch cơ bản.
Phenolphthalein hòa tan nhẹ trong nước và thường được hòa tan trong rượu để sử dụng trong các thí nghiệm. Nó là một axit yếu, có thể mất ion H + trong dung dịch. Các phân tử phenolphthalein là không màu, và ion phenolphthalein là màu hồng. Khi một bazơ được thêm vào phenolphthalein, sự cân bằng ion phân tử ⇌ chuyển sang bên phải, dẫn đến ion hóa nhiều hơn như H + ion được loại bỏ. Điều này được dự đoán bởi nguyên tắc của Le Chatelier.
Sử dụng
Chỉ thị sửa
Việc sử dụng chung của Phenolphthalein là một chỉ thị trong việc chuẩn độ axit-bazơ. Nó cũng là một thành phần của chỉ thị phổ quát, cùng với methyl đỏ, bromothymol xanh, và thymol xanh.
Phenolphthalein thông qua bốn trạng thái khác nhau trong dung dịch nước: Dưới điều kiện axit rất mạnh, nó tồn tại ở dạng proton, tạo màu cam. Giữa các điều kiện cơ bản mạnh và nhẹ, dạng lactone không màu. Mẫu phenolate deprotonated đơn (dạng anion của phenol) cho màu hồng quen thuộc. Trong các giải pháp cơ bản, màu hồng của phenolphthalein trải qua phản ứng giảm dần và trở nên không màu hoàn toàn trên 13,0 độ pH. Phản ứng chậm dần dần tạo ra ion (OH) 3 không màu Trong đôi khi được sử dụng trong các lớp học để nghiên cứu động học phản ứng.
| Species | H3In+ | H2In | In2− | In(OH)3− |
|---|---|---|---|---|
| Structure |  |
 |
 |
 |
| Model | 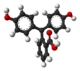 |
 |
 |
 |
| pH | <0 | 0−8.2 | 8.2−12.0 | >13.0 |
| Conditions | strongly acidic | acidic or near-neutral | basic | strongly basic |
| Color | orange | colorless | pink to fuchsia | colorless |
| Image |  |
 |
 |
| An animation of the pH dependent reaction mechanism: H3In+ → H2In → In2− → In(OH)3− |
Độ nhạy pH của Phenolphthalein được khai thác trong các ứng dụng khác: Bê tông có pH tự nhiên cao do canxi hydroxit hình thành khi xi măng Portland phản ứng với nước. Khi bê tông phản ứng với CO2 trong khí quyển, pH sẽ giảm xuống còn 8,5-9. Khi một dung dịch phenolphthalein 1% được áp dụng cho bê tông thông thường, nó sẽ chuyển thành màu hồng sáng. Tuy nhiên, nếu nó không màu, nó cho thấy rằng bê tông đã trải qua cacbon hóa. Trong một ứng dụng tương tự, spackling được sử dụng để sửa chữa các lỗ trong vách thạch cao chứa phenolphthalein. Khi được áp dụng, vật liệu tráng cơ bản vẫn giữ được màu hồng; khi vết xước đã được xử lý bằng phản ứng với carbon dioxide trong khí quyển, màu hồng sẽ biến mất
Phenolphthalein được sử dụng trong đồ chơi, ví dụ như một thành phần của thuốc biến mất, hoặc thuốc nhuộm biến mất trên tóc Hair Barbie của Hollywood. Trong mực in, nó được trộn với natri hydroxyd, phản ứng với carbon dioxide trong không khí. Phản ứng này dẫn đến độ pH giảm xuống dưới ngưỡng thay đổi màu vì các ion hydro được giải phóng bởi phản ứng:
OH- (aq) + CO2 (g) → CO2-3 (aq) + H + (aq)
Để phát triển kiểu tóc và các mô hình đồ hoạ “kỳ diệu”, mực in phun dung dịch hydroxit, dẫn đến sự xuất hiện của đồ hoạ ẩn cùng một cơ chế được mô tả ở trên để thay đổi màu trong dung dịch kiềm. Các mô hình cuối cùng sẽ biến mất một lần nữa vì phản ứng với carbon dioxide. Thymolphthalein được sử dụng cho cùng mục đích và theo cách tương tự, khi màu xanh là mong muốn

Sử dụng y tế
Phenolphthalein đã được sử dụng trong hơn một thế kỷ như thuốc nhuận tràng, nhưng hiện nay đang được loại bỏ nhờ thuốc nhuận tràng bán tự do vì những lo ngại về chất gây ung thư Thymolphthalein là thuốc nhuận tràng có liên quan được làm từ thymol. Xem Phenolsulfonphthalein cũng có.
Mặc dù có những mối quan ngại về khả năng gây ung thư, việc sử dụng phenolphthalein làm thuốc nhuận tràng có thể không gây ra ung thư buồng trứng. Phenolphthalein đã được tìm thấy để ức chế sự xâm nhập canxi của tế bào ở người qua lối vào canxi hoạt động ở cửa tiệm (SOCE, xem Kênh hoạt hóa canxi § Cấu trúc). Điều này được thực hiện bởi thuốc ức chế thrombin và thapsigargin, hai chất kích hoạt của SOCE làm tăng canxi nội bào miễn dịch
Một dạng thuốc giảm phenolphthalein, phenolphthalin, không màu, được sử dụng trong một bài kiểm tra để xác định chất có chứa máu, thường được gọi là bài kiểm tra Kastle-Meyer. Một mẫu khô được thu thập bằng giấy thấm hoặc giấy lọc. Một vài giọt rượu, sau đó một vài giọt phenolphthalin, và cuối cùng một vài giọt hydrogen peroxide được giọt vào mẫu. Nếu mẫu có chứa hemoglobin, nó sẽ trở thành màu hồng ngay lập tức khi bổ sung peroxit, vì thế hệ phenolphthalein. Một xét nghiệm dương tính cho biết mẫu có chứa hemoglobin, và do đó, có khả năng là máu. Một dương tính giả có thể là kết quả của sự có mặt của các chất có hoạt tính xúc tác tương tự như heme. Thử nghiệm này không phá hủy mẫu; nó có thể được giữ và sử dụng trong các bài kiểm tra thêm. Thử nghiệm này có cùng phản ứng với máu từ bất kỳ động vật nào, vì vậy cần phải kiểm tra thêm để xác định xem nó có nguồn gốc từ con người hay không.
Tổng hợp
Phenolphthalein có thể được tổng hợp bằng cách ngưng tụ anhydrit phthalic với hai chất tương đương phenol trong điều kiện axit (do đó tên). Nó được phát hiện năm 1871 bởi Adolf von Baeye
